이 페이지에서
Biocytogen은 새로운 약물 후보물질의 치료 가능성을 평가하기 위해 고품질의 in vivo 효능 연구를 수행하는 것을 전문으로 합니다. 이 연구는 인간의 타겟 유전자가 해당 마우스 유전자 위치에 삽입된 유전자 변형 마우스 모델, 중증 면역 결핍(B-NDG) 마우스 및 그 변형체, 그리고 야생형 모델을 활용합니다. 우리의 접근법은 종양학, 면역 종양학, 자가면역 및 염증성 질환, 대사 장애, 신경 질환 등의 약물 발견 및 개발을 지원합니다.
단일 및 이중 특이적 항체, 재조합 단백질, 항체-약물 결합체(ADC), 펩티드, 종양 백신, CAR-T 세포 치료, 종양용 바이러스 등 다양한 생물학적 제제의 테스트에 대한 전문성을 바탕으로 Biocytogen은 치료 효능에 대한 종합적인 평가를 보장합니다.
우리의 in vivo 모델은 다음을 포함합니다:



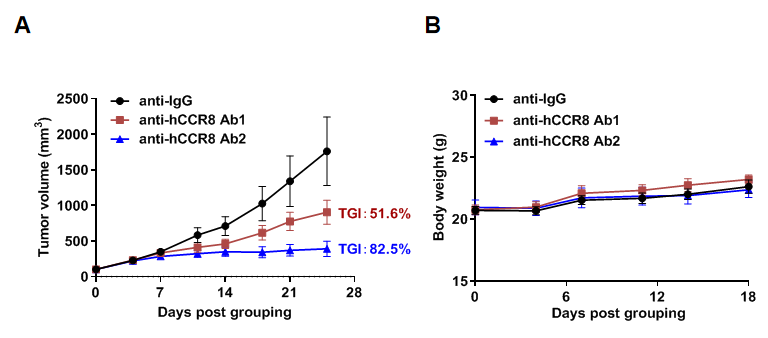
B-hCCR8 마우스에서 MC38 세포에 대한 항인간 CCR8 항체의 항종양 효과. 대장암 MC38 세포는 동형 B-hCCR8 마우스(여성, 7주령, n=6)에 피하 이식되었습니다. 종양 부피가 약 100 mm3에 이를 때, 마우스를 그룹화하여 항인간 CCR8 항체(자체 제작)를 투여했습니다. (A) 종양 성장 곡선. (B) 치료 중 체중 변화. 그림에서 보듯이, 항인간 CCR8 항체는 B-hCCR8 마우스에서 종양 성장을 효과적으로 억제했습니다. B-hCCR8 마우스는 항인간 CCR8 항체의 in vivo 평가를 위한 강력한 전임상 모델을 제공합니다. 값은 평균 ± SEM으로 표시됩니다.
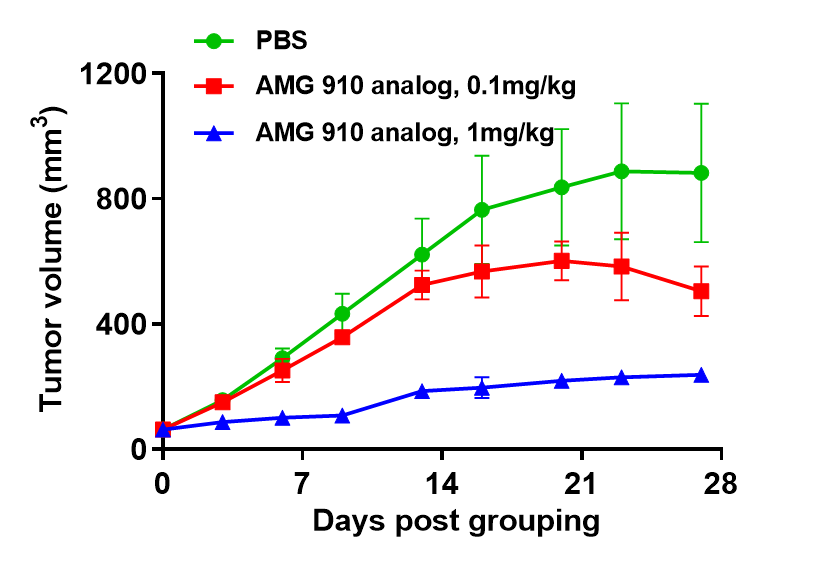
인간 면역 시스템 재구성 모델에서 이중 특이적 항체의 효능 평가.(A) CD3 기반 이중 특이적 항체 연구를 위한 인간 면역 시스템 재구성 모델. 인간 PBMC(5E6)를 정맥 주입한 후, NUGC4 세포(5E6)를 피하 이식하여 B-NDG 마우스에 투여했습니다. 항인간 CD3×Claudin18.2 이중 특이적 항체(AMG 910 유사물)는 인간 PBMC로 재구성된 B-NDG 마우스에서 NUGC4 종양 성장을 유의미하게 억제했습니다.
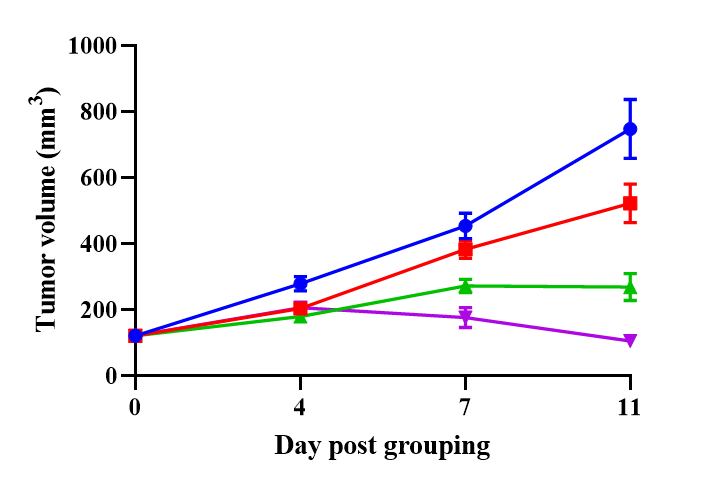
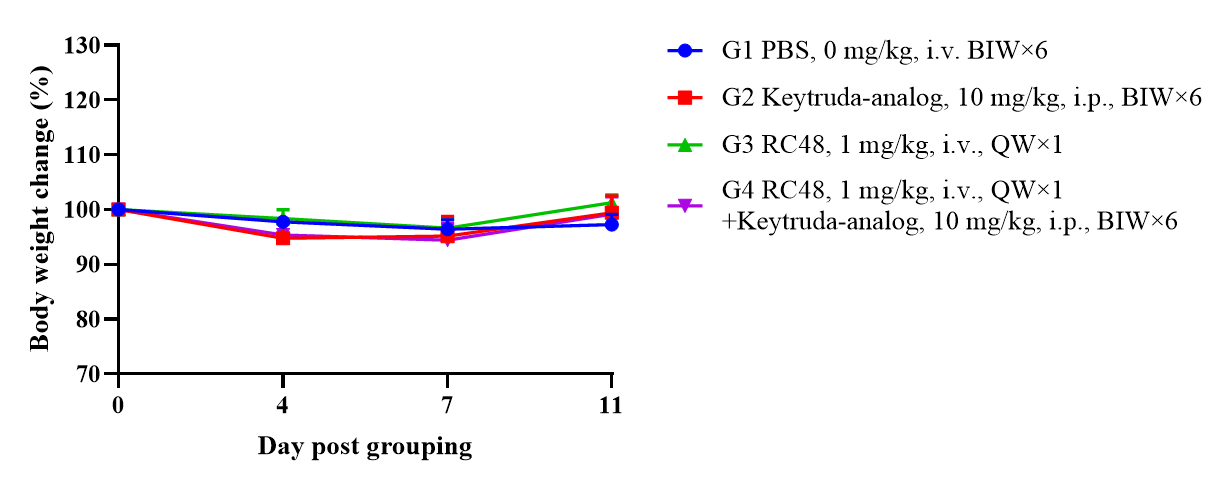
PBMC로 재구성된 B-NDG 마우스를 이용한 HER2-ADC 효능 연구
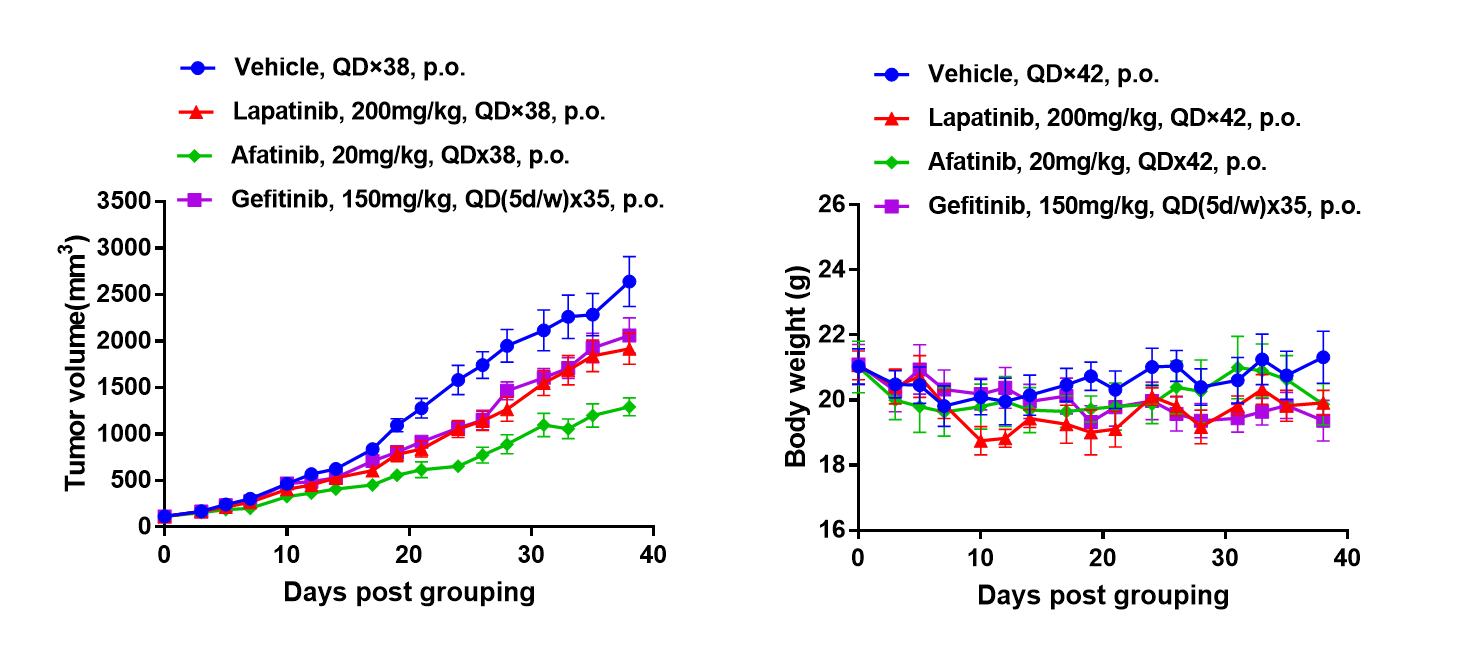
EGFR을 표적한 약물이 B-NDG 마우스에서 항종양 효과를 나타냄. (A) 분자 표적 소분자 항암 약물이 BP0062의 B-NDG 마우스에서 종양 성장을 약간 억제함. BP0062의 PDX 모델을 B-NDG 마우스(여성, 6주령, n=6)에 피하 이식했습니다. 종양 크기가 약 100 mm3에 이를 때, 마우스를 그룹화하여 패널에 표시된 다양한 표적 약물과 치료 계획에 따라 치료를 시작했습니다. (B) 치료 중 체중 변화. 패널 A에 나타난 바와 같이, 분자 표적 소분자 항암 약물은 효과적이며, BP0062의 PDX 모델은 종양 모델을 확립하고, EGFR 양성 세포를 가진 강력한 전임상 췌장 종양 모델을 제공함을 시사합니다. 값은 평균 ± SEM으로 표시됩니다.
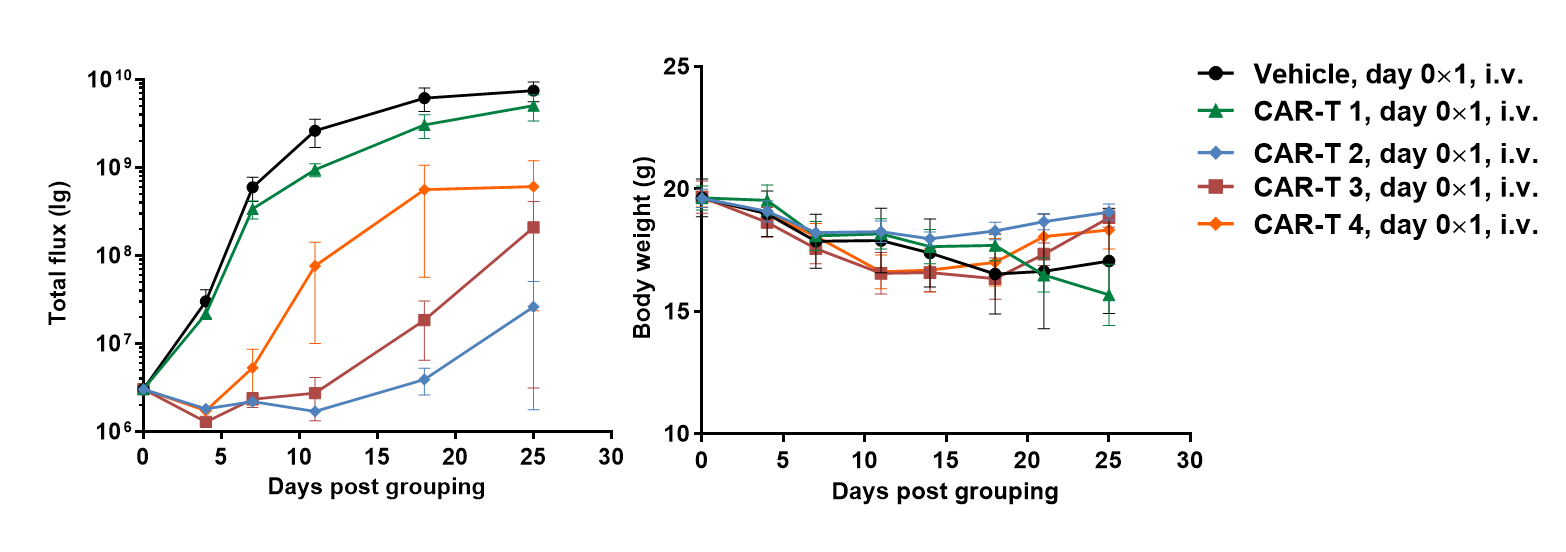
B-NDG 마우스를 이용하여 Raji 림프종 마우스 모델을 확립하고 항인간 CD47 항체의 효과를 검증했습니다. B-luc-GFP Raji 세포(5×105)를 꼬리 정맥으로 B-NDG 마우스에 주입했습니다. In vivo 이미징 시스템(IVIS)을 사용하여 종양 성장을 관찰했습니다. 종양의 형광 강도가 약 1×106 p/sec에 도달할 때, 동물을 대조군과 세 가지 치료군(n=6)으로 나누었습니다. (A) 종양 세포의 형광 강도 곡선; (B) 체중. 결과는 세 가지 항인간 CD47 항체가 모두 종양 성장을 유의미하게 억제할 수 있음을 보여주었습니다. B-NDG 마우스는 항인간 CD47 항체의 효과를 검증하는 강력한 모델을 제공합니다. 값은 평균 ± SEM으로 표시됩니다.