이 페이지에서
동맥경화는 혈관 내피 기능 장애, 염증 세포 침윤, 동맥경화성 플라크의 점진적 형성이 특징인 만성 염증성 질환입니다. 동맥경화 과정에서 지방 대사 장애(저밀도 지단백(LDL) 증가 및 고밀도 지단백(HDL) 감소)는 동맥경화성 플라크 형성을 초래할 수 있습니다.
Biocytogen은 지방 대사를 타겟으로 한 인간화 마우스를 개발하여 항체 및 핵산 약물과 같은 새로운 치료제를 테스트하고, 질병 메커니즘을 연구하기 위한 유전자 녹아웃 모델을 개발했습니다.
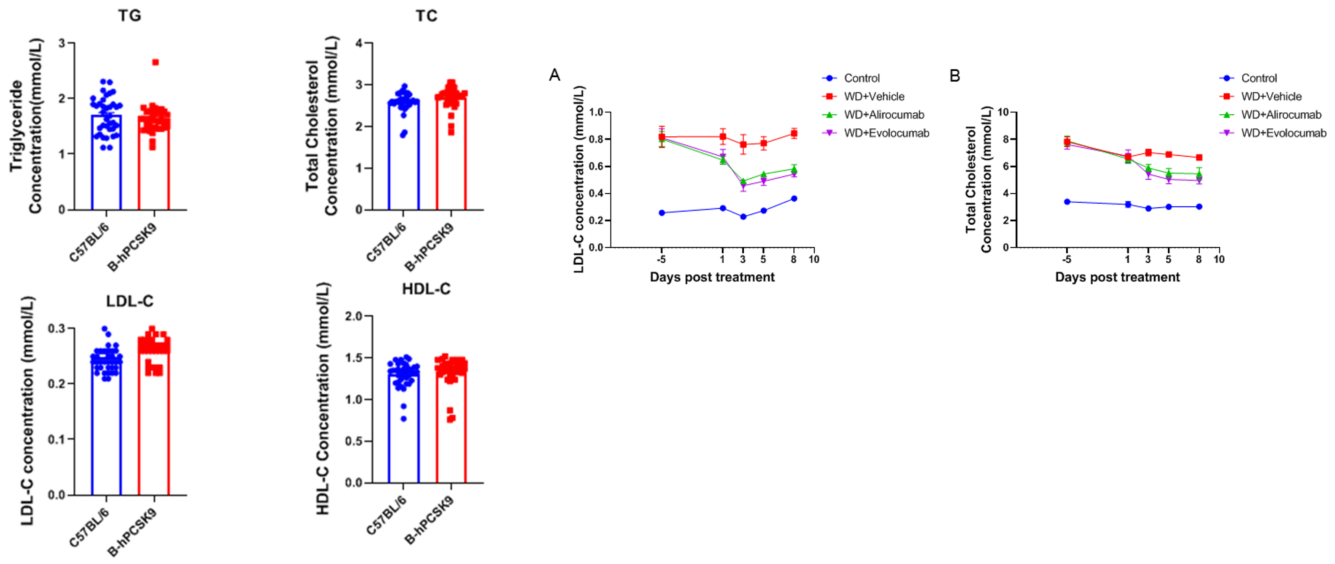
항인간 PCSK9 항체는 B-hPCSK9 마우스에서 지방 대사를 개선했습니다. C57BL/6 야생형 및 B-hPCSK9 마우스는 6주간 서양식 식단 유도 후 Alirocumab(사내 제조) / Evolocumab(사내 제조) 또는 아이소타입 대조 항체(단회 투여, 피하주사)(n = 8)로 처리되었습니다. 혈액은 -5일, 1일, 3일, 5일, 8일에 수집되어 분석되었습니다. 항인간 PCSK9 항체 처리 그룹에서는 LDL-C(A)와 TC(B)의 혈청 수준이 아이소타입 대조군에 비해 감소했습니다. 결과는 항인간 PCSK9 항체가 B-hPCSK9 마우스에서 혈중 지방 조절에 효과적임을 시사합니다. 값은 평균 ± 표준 오차(SEM)로 표시됩니다. TC, 총 콜레스테롤; LDL-C, 저밀도 지단백 콜레스테롤.
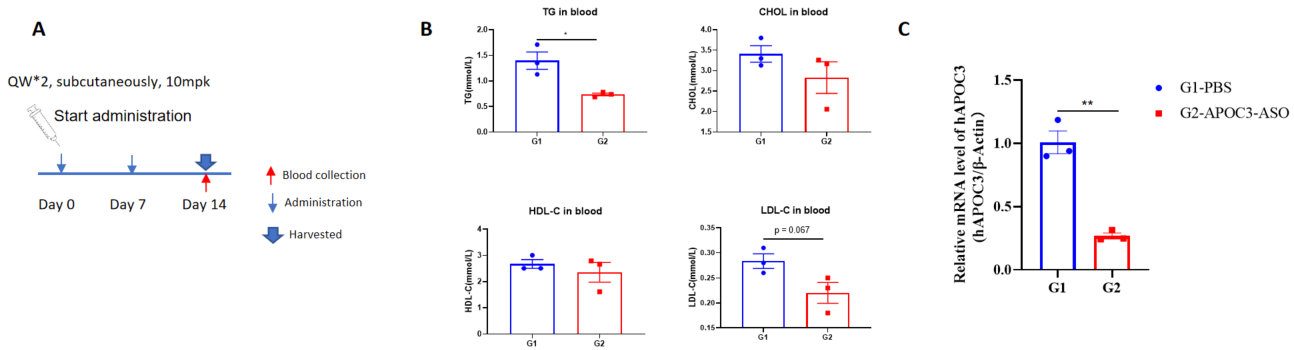
B-hAPOC3 마우스에서 인간 APOC3에 대한 핵산 약물의 억제 효율. B-hAPOC3 마우스는 두 그룹(n = 3/그룹, 6주령)으로 무작위 배정되었습니다. 인간 APOC3를 타겟으로 한 핵산 약물(특허에 따라 합성)과 PBS가 각기 마우스에 투여되었습니다. 핵산 약물은 PBS 수용액 형태로 투여되었습니다. 모든 동물의 약물 용량은 체중을 기준으로 계산되었습니다. 마우스는 14일째에 희생되었으며, 간 조직을 수집하여 qPCR로 인간 APOC3 mRNA의 발현 수준을 측정했습니다. A, 실험 처리 도식. B, 치료 후 B-hAPOC3 마우스의 혈중 지방 수준. 대조군(G1)과 비교하여 치료군(G2)은 TG가 유의미하게 감소했습니다. C, 간에서 인간 APOC3 mRNA의 발현. 치료군(G2)에서 인간 APOC3는 대조군(G1)과 비교하여 유의미하게 감소하였으며, 억제율은 73.4%였습니다. 이는 B-hAPOC3 마우스가 인간 APOC3 타겟 핵산 약물의 체내 평가를 위한 강력한 전임상 모델을 제공함을 보여줍니다. 값은 평균 ± 표준 오차(SEM)로 표시됩니다.
ApoE-/- 마우스에서의 특수 식이유도 동맥경화 모델 확립
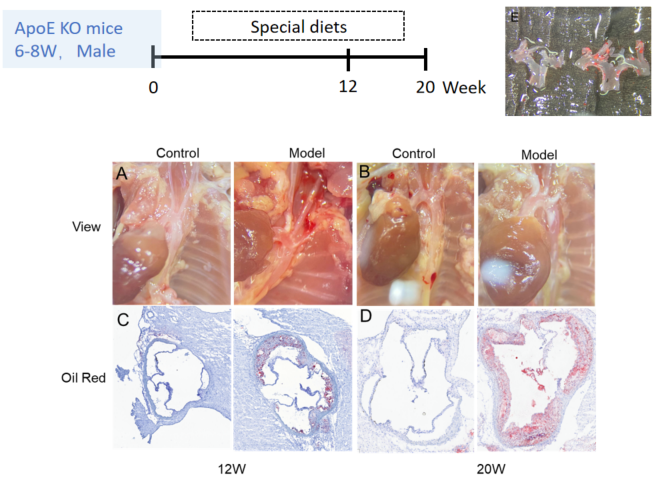
특수 식이유도 동맥경화 모델 확립. A-B, 12주 및 20주 마우스에서의 동맥경화성 플라크. C-D, 12주 및 20주 대동맥 동의 오일 레드 결과. E, 12주 대동맥 궁의 조직 염색. 각 그룹의 N = 8마리.
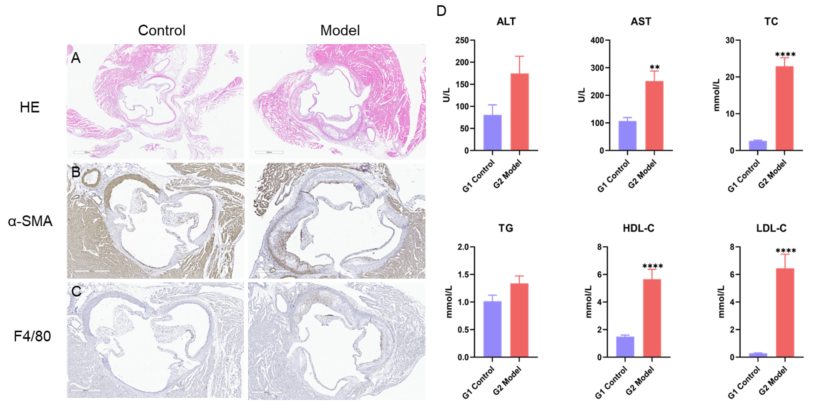
12주 동맥경화 모델에서의 조직 염색 및 혈액 생화학 결과 A, 대동맥 동의 H&E 결과. B-C, 면역조직화학에서 α-SMA 및 F4/80 발현. D, 혈청에서 ALT, AST, TC, TG, HDL-C, LDL-C 수준. 값은 평균 ± 표준 오차(SEM)로 표시됩니다. 각 그룹의 N = 8마리. **p<0.01, ****p<0.0001.